Salicylaldehyd
| Salicylaldehyd | |
|---|---|
 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | 2-hydroxybenzenkarbaldehyd |
| Ostatní názvy | 2-hydroxybenzaldehyd, o-hydroxybenzaldehyd, aldehyd kyseliny salicylové |
| Sumární vzorec | C7H6O2 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 90-02-8 |
| ChEBI | 16008 |
| SMILES | O=Cc1ccccc1O |
| InChI | 1/C7H6O2/c8-5-6-3-1-2-4-7(6)9/h1-5,9H |
| Vlastnosti | |
| Molární hmotnost | 122,121 g/mol |
| Teplota tání | −7 °C (266 K) |
| Teplota varu | 196 až 197 °C (469 až 470 K) |
| Hustota | 1,146 g/cm3 |
| Bezpečnost | |
| [1] Varování[1] | |
| H-věty | H302 H315 H317 H319 H335 H411 |
| P-věty | P280 P305+351+338 |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Salicylaldehyd (IUPAC název 2-hydroxybenzaldehyd) je organická sloučenina patřící mezi aromatické aldehydy, je společně s 3-hydroxybenzaldehydem a 4-hydroxybenzaldehydem jedním z izomerů hydroxybenzaldehydu. Jedná se o olejovitou bezbarvou kapalinu, která má ve vyšších koncentracích zápach připomínající hořké mandle. Používá se na přípravu chelatačních činidel, z nichž některá jsou průmyslově významná.
Příprava
Salicylaldehyd se připravuje Reimerovou–Tiemannovou reakcí, tedy zahříváním fenolu a chloroformu s hydroxidem sodným nebo draselným:
Také jej lze získat kondenzací fenolu nebo jeho derivátů s formaldehydem za vzniku 2-hydroxybenzylalkoholu a následnou oxidací na aldehyd.
Deriváty salicylaldehydu lze připravit z fenolových derivátů Duffovou reakcí nebo působením paraformaldehydu za přítomnosti chloridu hořečnatého a zásady.[2]
Výskyt
Salicylaldehyd vytváří aroma pohanky.[3]
Je také jednou ze složek kastorea. Rovněž se nachází ve výměšcích larev některých druhů mandelinek,[4] jako je například mandelinka topolová.
Reakce a použití
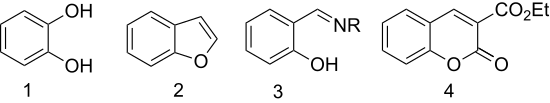
Salicylaldehyd se používá na výrobu těchto látek:
- Katecholu oxidací pomocí peroxidu vodíku.[5]
- Benzofuranu etherifikací s kyselinou chloroctovou a následnou cyklizací (první krok tohoto postupu se nazývá Rapova–Stoermerova kondenzace).[6][7][8]
- Chelatačních činidel reakcemi s aminy.
- 3-karbethoxykumarinu (derivátu kumarinu) aldolovou kondenzací.[9]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Salicylaldehyde na anglické Wikipedii.
- ↑ a b Salicylaldehyde. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ TROND VIDAR HANSEN; LARS SKATTEBØL. Ortho-Formylation of Phenols; Preparation of 3-Bromosalicylaldehyde. Org. Synth.. 2005, s. 64. (anglicky)
- ↑ D. Janeš; S. Kreft. Salicylaldehyde is a characteristic aroma component of buckwheat groats. Food Chemistry. 2008, s. 293–298. PMID 26003350.
- ↑ Pauls, G., Becker, T., et al. (2016). Two Defensive Lines in Juvenile Leaf Beetles; Esters of 3-nitropropionic Acid in the Hemolymph and Aposematic Warning. Journal of Chemical Ecology 42 (3) 240-248.
- ↑ DAKIN, H. D. Catechol. Org. Synth.. 1923, s. 28. Dostupné online. (anglicky); Coll. Vol.. S. 149. (anglicky)
- ↑ E. Rap. Sull' α-Benzoilcumarone. Gazzetta Chimica Italiana. 1895, s. 285–290.
- ↑ R. Stoermer. Synthesen und Abbaureactionen in der Cumaronreihe. Liebig's Annalen der Chemie. 1900, s. 237–336. Dostupné online.
- ↑ BURGSTAHLER, A. W.; WORDEN, L. R. Coumarone. Org. Synth.. 1966, s. 28. Dostupné online. (anglicky); Coll. Vol.. S. 251. (anglicky)
- ↑ HORNING, E. C.; HORNING, M. G.; DIMMIG, D. A. 3-Carbethoxycoumarin. Org. Synth.. 1948, s. 24. Dostupné online. (anglicky); Coll. Vol.. S. 165. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu Salicylaldehyd na Wikimedia Commons
Obrázky, zvuky či videa k tématu Salicylaldehyd na Wikimedia Commons  Encyklopedické heslo Salicylový aldehyd v Ottově slovníku naučném ve Wikizdrojích
Encyklopedické heslo Salicylový aldehyd v Ottově slovníku naučném ve Wikizdrojích
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for substances hazardous to human health.
salicylaldehyde; o-Formylphenol; o-Hydroxybenzaldehyde; Salicylal
Autor: Nuklear, Licence: CC BY-SA 4.0
from the left: catechol, benzofuran, a salicylaldehydimine (R = alkyl or aryl), 3-carbethoxycoumarin.








