Tetrachloroplatnatan draselný
| Tetrachloroplatnatan draselný | |
|---|---|
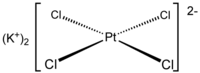 Strukturní vzorec | |
| Obecné | |
| Systematický název | tetrachloroplatnatan draselný |
| Sumární vzorec | K2PtCl4 |
| Vzhled | červená pevná látka |
| Identifikace | |
| Registrační číslo CAS | 10025-99-7 |
| EC-no (EINECS/ELINCS/NLP) | 233-050-9 |
| PubChem | 61440 |
| SMILES | Cl[Pt-2](Cl)(Cl)Cl.[K+].[K+] |
| InChI | 1S/4ClH.2K.Pt/h4*1H;;;/q;;;;2*+1;+2/p-4 |
| Vlastnosti | |
| Molární hmotnost | 415,09 g/mol |
| Teplota tání | 265 °C (538 K) |
| Hustota | 3,38 g/cm3 |
| Rozpustnost ve vodě | 0,93 g/100 ml (16 °C) 5,3 g/100 ml (100 °C) |
| Bezpečnost | |
| [1] | |
| H-věty | H301 H315 H317 H318 H334}[1] |
| P-věty | P261 P264 P270 P272 P280 P285 P301+310 P302+352 P304+341 P305+351+338 P310 P321 P330 P332+313 P333+313 P342+311 P362 P363 P405 P501[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Tetrachloroplatnatan draselný je anorganická sloučenina se vzorcem K2PtCl4, používaná na přípravu dalších komplexů platiny. Její molekula se skládá z draselných kationtů a čtvercově rovinného dianiontu PtCl42−. Podobnými solemi jsou například tetrachloroplatnatan sodný (Na2PtCl4), který je rozpustný v alkoholech, a kvartérní amoniové soli, rozpustné ve větším počtu organických rozpouštědel.
Příprava
Tetrachloroplatnatan draselný se připravuje redukcí hexachloroplatiničitanu draselného oxidem siřičitým.[2]
K2PtCl4 je jednou z forem platiny nejsnáze získatelných z platinových rud. Komplex se dostatečně rozpouští pouze ve vodě. Přidáním alkoholů, obzvláště za přítomnosti zásady, dojde k redukci na platinu. Organické tetrachloroplatnatany, například [PPN]2PtCl4, jsou rozpustné v chlorovaných uhlovodících.[3]
Reakce
Chloridové ligandy v [PtCl4]2− mohou být nahrazeny mnoha jinými ligandy. Reakcí s trifenylfosfinem se [PtCl4]2− mění na cis-bis(trifenylfosfin)chlorid platnatý:
- PtCl42− + 2 PPh3 → cis-PtCl2(PPh3)2 + 2 Cl−
Protinádorové léčivo cisplatina se dá připravit podobně:[2]
- PtCl42− + 2 NH3 → cis-PtCl2(NH3)2 + 2 Cl−
Endithioláty mohou z PtCl42− odštěpit všechny čtyři chloridové ligandy za vzniku bis(dithiolen)ových komplexů.[4]
Redukcí vzniká koloidní platina, která může být využita v katalýze.[5]
V minulosti měla velký význam reakce [PtCl4]2− s amoniakem. Jejím produktem je tmavě zelená sraženina o stewchiometrickém vzorci PtCl2(NH3)2. Tato látka, nazývaná Magnusova zelená sůl, funguje jako polovodivý koordinační polymer tvořený řetězci střídajících se iontů [PtCl4]2− a [Pt(NH3)4]2+.
Reference
V tomto článku byl použit překlad textu z článku Potassium tetrachloroplatinate na anglické Wikipedii.
- ↑ a b c https://pubchem.ncbi.nlm.nih.gov/compound/61440
- ↑ a b R. N. Keller. Potassium Tetrachloroplatinate(II). Inorganic Syntheses. 1963, s. 247–250. ISBN 9780470132333. DOI 10.1002/9780470132333.ch79.
- ↑ L. I. Elding; A. Oskarsson; V. Yu. Kukushkin. Platinum Complexes Suitable as Precursors for Synthesis in Nonaqueous Solvents. Inorganic Syntheses. 1997, s. 276–279. ISBN 9780470132623. DOI 10.1002/9780470132623.ch47.
- ↑ Scott D. Cummings; Richard Eisenberg. Acid-Base Behavior of the Ground and Excited States of Platinum(II) Complexes of Quinoxaline-2,3-dithiolate. Inorganic Syntheses. 1995, s. 3396–3403. DOI 10.1021/ic00117a005.
- ↑ T. S. Ahmadi; Z. L. Wang; T. C. Green; A. Henglein; M. A. El-Sayed. Shape-Controlled Synthesis of Colloidal Platinum Nanoparticles. Science. 1996, s. 1924–1926. DOI 10.1126/science.272.5270.1924. PMID 8662492.
- ↑ W. Caseri. Derivatives of Magnus' green salt; from intractable materials to solution-processed transistor. Platinum Metals Review. 2004, s. 91–100. DOI 10.1595/147106704X1504.
Externí odkazy
 Obrázky, zvuky či videa k tématu Tetrachloroplatnatan draselný na Wikimedia Commons
Obrázky, zvuky či videa k tématu Tetrachloroplatnatan draselný na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for toxic substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for substances hazardous to human health.
chemical structure of K2PtCl4








