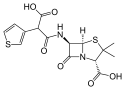
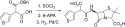Tikarcilin
| tikarcilin | |
|---|---|
 | |
| Název (INN) | ticarcillin (angličtina) |
| Kódy | |
| Číslo CAS | 34787-01-4 |
| ChEMBL ID | CHEMBL1449 |
| ChemSpider ID | 33876 |
| PubChem | 36921 |
| Chemie | |
| Sumární vzorec | C₁₅H₁₆N₂O₆S₂ |
| SMILES | CC1(C(N2C(S1)C(C2=O)NC(=O)C(C3=CSC=C3)C(=O)O)C(=O)O)C |
| InChI | InChI=1S/C15H16N2O6S2/c1-15(2)9(14(22)23)17-11(19)8(12(17)25-15)16-10(18)7(13(20)21)6-3-4-24-5-6/h3-5,7-9,12H,1-2H3,(H,16,18)(H,20,21)(H,22,23)/t7-,8-,9+,12-/m1/s1 |
| Molární hmotnost | 384,044 978 Da |
| Farmakologie | |
| Indikace | upper respiratory tract infection, sepse, infekce močových cest, gram-negative bacterial infection, skin infection a Pseudomonas infection |
| Některá data mohou pocházet z datové položky. | |
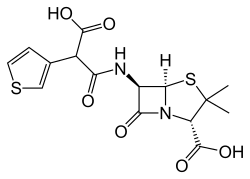
Tikarcilin (angl. ticarcillin) řadíme mezi karboxypeniciliny. Je téměř vždy vyráběný a užívaný v kombinaci s kyselinou klavulanovou jako tikarcilin / klavulanová kyselina. Jelikož se jedná o penicilin, patří spadá do větší třídy beta-laktamových antibiotik. Klinicky je nejčastěji užíván jako injekční antibiotikum pro léčbu vyvolanou gramnegativními bakteriemi, zejména Pseudomonas aeruginosa. Pro léčbu pseudomonádových infekcí je často kombinován s dalšími antibiotiky, např. s aminoglykosidovým antibiotikem gentamicinem. Tikarcilin je také jedním z mála antibiotik účinných při léčbě infekce vyvolaných Stenotrophomonas maltophilia. Jeho spektrum účinnosti je však shodné s karbenicilinem, je však několikanásobně účinnější na kmeny Enterobacter spp., Proteus vulgaris a Bacteroides fragillis. Méně účinný je na G+ koky. Rezistentní jsou bakterie z rodu Enterococcus a Klebsiella.[1][2]
Je dodáván jako bílý nebo světle žlutý prášek, který je snadno rozpustný ve vodě, ale měl by být rozpuštěn pouze těsně před použitím, aby se zabránilo jeho degradaci.
Materia medica: Ticarcillinum, Ticarcillinum dinatricum, Ticarcillinum dinatricum pro injectione [1]
Byl patentován v roce 1963.[3]
Mechanismus účinku
Baktericidní účinky tikarcilinu vyplývají z jeho schopnosti zabránit zesíťovatění peptidoglykanu během syntézy buněčné stěny, v okamžiku bakteriálního dělení, což způsobují smrt bakterie.
Tikarcilin, stejně jako penicilin, obsahuje β-laktamový kruh. Ten je možné štěpit bakteriálními beta-laktamázami, což má za následek inaktivaci antibiotika. Bakterie, které mohou produkovat β-laktamázy, jsou proto rezistentní na β-laktamová antibiotika. Proto je tikarcilin často kombinován s inhibitory β-laktamázy, jako je kyselina klavulanová (ko-tikarclav). Tikarcilin může částečně díky běžnému beta-laktamovému kruhu vyvolat u pacientů alergických na penicilin reakce. Dalšími vedlejšími reakce mohou být nauzea, průjem a lokální zarudnutí kůže.[2]
Další použití
V molekulární biologii je tikarcilin používán jako alternativa k ampicilinu k testování absorpce markerových genů na bakterie. Zabraňuje výskytu satelitních kolonií, ke kterým dochází, když se ampicilin rozpadá v médiu. Také je užíván v rostlinné molekulární biologii, jelikož je schopen účinně likvidovat Agrobacterium, které je schopno předávat geny do rostlinných buněk.
Dávkování a podávání
Tikarcilin se neabsorbuje perorálně, proto musí být podáván intravenózní nebo intramuskulární injekcí. Následující dávky jsou určeny pro kombinaci trikarcilin s kyselinou klavulanovou.
Pes, kočka: 40 – 100 mg/kg živé hmotnosti nitrožilně či nitrosvalově každých 4–6 hodin
Drobní hlodavci (králík, činčila, křeček, morče, pískomil): nepoužívá se
Ptáci: 150 – 200 mg/kg živé hmotnosti nitrožilně či nitrosvalově každých 8–12 hodin [2]
Obchodní názvy a přípravky
- Tikarcilin: Ticar dříve uváděl na trh Beecham, poté SmithKline Beecham až do roku 1999, kdy se spojil s Glaxo a vytvořil GlaxoSmithKline; ve Velké Británii již není k dispozici. Americká distribuce skončila v roce 2004. Ticar byl nahrazen Timentinem. Na rozdíl od Ticarinu však Timentin obsahuje klavulanát. Stabilita rekonstituovaného tikarcilin klavulanátu je 48–72 hodin.
- Tikarcilin / klavulanát: Timentin v Austrálii, Velké Británii a USA prodával Beecham, poté GlaxoSmithKline.
- V České republice není v současnosti (podzim 2019) registrován žádný léčivý přípravek s obsahem tikarcilinu ani pro lidské, ani pro veterinární užití.
Syntéza
Karbenicilin se v lékařství používá především kvůli nízké toxicitě a použitelnosti při léčbě infekcí močových cest způsobených citlivými druhy Pseudomonas . Díky nízké účinnosti, nízké orální aktivitě a náchylnosti k bakteriálním beta-laktamázám je často k nahrazován látkami bez těchto deficitů. Jednou z jeho náhrad je tikarcilin. Jeho vznik vycházel z dobře známé skutečnosti, že dvojmocná síra je zhruba ekvivalentní vinylové skupině (např. methiopropamin, sufentanil, pizotylin atd.).

Syntéza začíná tím, že je připraven monobenzylester kyseliny 3-thienylmalonové, který se převádí na kyselý chlorid účinkem SOCl2 a ten pak kondenzuje s kyselinou 6-aminopenicillanovou (6-APA). Následná hydrogenolýza (Pd/C) dokončuje syntézu tikarcilinu.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Ticarcillin na anglické Wikipedii.
- ↑ a b ŠIMŮNEK, Jan; SMOLA, Jiří. Antibiotika, sulfonamidy a chinolony ve veterinární medicíně. 1. vyd. Tišnov: LAST STEINHAUSER, s.r.o., 1998. 136 s. ISBN 80-900260-6-0. S. 27–28.
- ↑ a b c BSAVA Small Animal Formulary Part A: Canine and Feline. www.bsavalibrary.com [online]. [cit. 2019-10-18]. Dostupné online. (anglicky)
- ↑ IUPAC; FISCHER, János; GANELLIN, C. Robin. Analogue-based Drug Discovery. [s.l.]: John Wiley & Sons 610 s. Dostupné online. ISBN 9783527607495. (anglicky) Google-Books-ID: FjKfqkaKkAAC.
- ↑ Espacenet - Bibliographic data. worldwide.espacenet.com [online]. [cit. 2019-10-18]. Dostupné online.
Externí odkazy
 Obrázky, zvuky či videa k tématu tikarcilin na Wikimedia Commons
Obrázky, zvuky či videa k tématu tikarcilin na Wikimedia Commons