Tritium
| Tritium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Svítící přívěsek s luminoforem a tritiovou náplní | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Obecné | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Název, značka, číslo | Tritium, T, 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cizojazyčné názvy | lat. Tritium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupina, perioda, blok | 1. skupina, 1. perioda, blok s | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemická skupina | Nekovy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | bezbarvý plyn | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Registrační číslo CAS | 10028-17-8 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Relativní atomová hmotnost | 3,016 049 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronová konfigurace | 1s1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidační čísla | −I, I | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mechanické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hustota | 0,281 g/dm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenství | plynné | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 134 W·m−1·K−1 (30 K, kapalina) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termodynamické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota tání | −252,5 °C (20,65 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota varu | −248,11 °C (25,04 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota trojného bodu T3 | −252,53 °C (20,62 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak trojného bodu p3 | 21,55 kPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritická teplota Tk | −229 °C (44,15 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izotopy | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| triton (t, 3H+, T+) | |
|---|---|
 | |
| Obecné vlastnosti | |
| Klasifikace | složená částice (atomové jádro) |
| Složení | p + 2×n |
| Antičástice | antitriton (p + 2×n) |
| Fyzikální vlastnosti | |
| Klidová hmotnost | 2808,921 136 68(88)[1] MeV/c2 5,007 356 7512(16) × 10−27[1] kg |
| Elektrický náboj | +1 e 1,602 176 634 × 10−19[1] C |
| Magnetický moment | 2,978 962 4650(59)[1] μN |
| Spin | ½ ħ |
Tritium je radioaktivní izotop vodíku (3H). Jádro tritia (jako částice se nazývá triton) obsahuje jeden proton a dva neutrony, zatímco normální vodíkové jádro sestává pouze z jednoho protonu. Jeho relativní atomová hmotnost je 3,016049. Za standardního tlaku a teploty je to plyn (T2 neboli 3H2).
Výskyt
Tritium se vlivem ionizujícího záření z vesmíru vyskytuje ve vrchních vrstvách zemské atmosféry a v malé míře je součástí emisí z jaderných elektráren. Významná množství vznikala při explozích jaderných zbraní. Z uvedených důvodů se tritium ve stopovém množství vyskytuje i v běžné vodě.[2]
Fyzikálně-chemické vlastnosti
Tritium je beta zářič (β−), při svém rozpadu produkuje elektron (e−), antineutrino (νe) a vzniká 3He. Poločas rozpadu je 12,32 let.
Někdy mu bývá přiřazována i chemická značka T, přestože se nejedná o jiný prvek. Ve sloučenině s kyslíkem tvoří tritiovou vodu T2O.
Nebezpečnost
I když jde o beta zářič, jeho nebezpečnost je jen minimální.[3][4] Záření tritia zastaví už 6 mm silná vrstva vzduchu. Určité nebezpečí by hrozilo pouze při jeho požití, vdechnutí nebo kontaminaci pokožky na citlivém místě.
Relativní bezpečnost tritia reflektoval v roce 2019 i Státní úřad pro jadernou bezpečnost, když opatřením obecné povahy prodejcům typově schválených výrobků GTLS, jejichž aktivita nepřesahuje 20 GBq, zrušil povinnost získání individuálního povolení k tomuto prodeji. V odůvodnění opatření Státní úřad pro jadernou bezpečnost dovozuje, že používání těchto výrobků nezpůsobí jejich uživatelům zvýšení efektivní dávky ionizujícího záření o více než 10 µSv/rok, což je považováno za zanedbatelnou hodnotu.
Využití
Tritia se využívá jako trvalého zdroje slabého světla, někdy označovaného jako GTLS (Gaseous Tritium Light Source). Plynné tritium je uzavřeno v skleněných mikrokapslích, na jejichž stěně je vrstva fosforeskující látky, která vlivem dopadajícího beta záření svítí. Obvykle se používá ZnS, u něhož je možné přidáním jiných látek měnit barvu světla. Nejintenzivnější je zelené světlo, ale zářič může svítit i žlutě, modře, fialově, červeně apod.[5]
Používá se na ciferníky hodinek, mířidla zbraní, jako přívěsky nebo nouzové svítilny.
Další obrázky
- Použití tritia v mířidlech
- (c) Metroplex, CC BY-SA 3.0Modré světlo
- Ciferník hodinek osvětlený tritiem
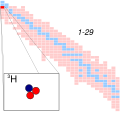
- Umístění tritia ve schématu izotopů
Reference
- ↑ a b c d Fundamental Physical Constants; 2022 CODATA recommended values. NIST, květen 2024. Dostupné online, PDF (anglicky)
- ↑ Frequently Asked Questions: Tritium [online]. Canadian Nuclear Safety Commission [cit. 2013-02-21]. Kapitola Q8. Dostupné v archivu pořízeném dne 2013-05-12. (anglicky)
- ↑ Nuclide Safety Data Sheet Hydrogen-3 [online]. [cit. 2006-11-09]. Dostupné v archivu pořízeném dne 2006-09-08.
- ↑ Opatření obecné povahy [online]. Praha: Státní úřad pro jadernou bezpečnost, 2019-10-21 [cit. 2021-12-04]. Dostupné online.
- ↑ Tritium, iluminace, GTLS – jak to celé funguje? [online]. TritiumShop [cit. 2013-02-21]. Dostupné online.
Související články
Externí odkazy
Média použitá na této stránce
Autor: Zagothal, Licence: CC BY-SA 4.0
Jádro tritia, obsahuje jeden proton a dva neutrony
Autor:
- Hydrogen-3.png: Created by oo64eva using Macromedia Fireworks 4.
- derivative work: Gregors (talk) 21:03, 12 March 2011 (UTC)
Hydrogen-3 or Tritium The table is a simplified version of w:Table of nuclides (complete). It contains isotopes arranged by proton number from left to right and by neutron number from top to down, where blue symbolizes stable isotopes and orange symbolizes unstable isotopes.
(c) Metroplex, CC BY-SA 3.0
PS90 Night sight reticle. Normally you will only see this reticule in darkness and it will appear red/orange from the Tritium illumination. I shined a light into the rear fiber optic to make it show up clearly. Author: Metroplex
(c) I, Autopilot, CC BY 2.5
Swiss Military Watch Commander model with tritium-illuminated face
Autor: Cgommel, Licence: CC BY-SA 2.0 de
A keychain containing a radioluminescent tritium vial (long exposure).