Trifenyl-fosfát
| Trifenylfosfát | |
|---|---|
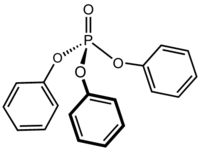 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | trifenyl-fosfát |
| Funkční vzorec | (C6H5O)3PO |
| Sumární vzorec | C18H15O4P |
| Vzhled | bezbarvé krystaly[1] |
| Identifikace | |
| Registrační číslo CAS | 115-86-6 |
| EC-no (EINECS/ELINCS/NLP) | 204-112-2 |
| PubChem | 8289 |
| ChEBI | 35033 |
| SMILES | O=P(Oc1ccccc1)(Oc2ccccc2)Oc3ccccc3 |
| InChI | 1S/C18H15O4P/c19-23(20-16-10-4-1-5-11-16,21-17-12-6-2-7-13-17)22-18-14-8-3-9-15-18/h1-15H |
| Vlastnosti | |
| Molární hmotnost | 326,28 g/mol |
| Teplota tání | 50,5 °C (323,6 K)[1] |
| Teplota varu | 370 °C (643 K)[1] |
| Hustota | 1,2055 g/cm3[1] (20 °C) |
| Rozpustnost ve vodě | nerozpustný[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v chloroformu, ethanolu a acetonu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v benzenu, diethyletheru a tetrachlormethanu[1] |
| Tlak páry | 1 Pa[1] (20 °C) |
| Bezpečnost | |
| [1] | |
| H-věty | H400 H410 H411[1] |
| P-věty | P273 P391 P501[1] |
| Teplota vzplanutí | 220 °C (493 K)[1] |
Některá data mohou pocházet z datové položky. | |
Trifenylfosfát (zkráceně TPhP) je organická sloučenina se vzorcem OP(OC6H5)3, triester kyseliny fosforečné a fenolu. Používá se jako plastifikátor a zpomalovač hoření.[2]
Příprava
Trifenylfosfát se připravuje SN2 reakcí oxychloridu fosforečného s fenolem.
Použití
Trifenylfosfát má využití jako zpomalovač hoření a plastifikátor.[3]
Jako zpomalovač hoření se přidává do řady výrobků, jako jsou elektronické přístroje, polyvinylchlorid, hydraulické kapaliny, lepidla, laky na nehty a lité pryskyřice. Účinkuje takto: Nejprve se tepelným rozkladem vytvoří kyselina fosforečná. Ta reaguje za tvorby kyseliny difosforečné, jež po kondenzaci zabraňuje přenosu tepla. Trifenylfosfát je účinný pouze v plynném skupenství.[4]
Jako plastifikátor se trifenylfosfát používá v lacích a hydraulických kapalinách. Nacházet se může mimo jiné v lacích na nehty.[5][6]
Toxicita
O významnějších toxických účincích TPhP existuje jen málo dat. Přestože se původně předpokládalo, že jsou jeho zdravotní účinky minimální, tak bylo později zjištěno, že nebezpečný může být. Trifenylfosfát má nízkou akutní toxicitu při styku s kůží nebo vstupu ústy.[2] Stále více studií ovšem ukazuje na reprodukční a vývojovou toxicitu, neurotoxicitu, narušování metabolismu, vliv na žlázy s vnitřní sekrecí a genotoxicitu.[5][7][8]
TPhP má také významné estrogenní účinky.[9][10]
Koncentrace vyšší než nejnižší, při kterých jsou pozorovatelné účinky, byly nalezeny v korálech a rybách. TPhP tak může být v prostředí přítomen v koncentracích dostatečně vysokých na to, aby měl na něj škodlivé vlivy.[10] TPhP je považován za „vysoce toxický“, pro vodní organismy s možnými dlouhodobými účinky.[11]
Ve srovnání s mnoha ostatními organickými znečišťujícími látkami má TPHP nízkou afinitu k lipidům, přesto u této sloučeniny dochází k bioakumulaci. Mechanismy vysvětlující akumulaci TPhP ovšem nejsou známy.[12]
Přeměny v životním prostředí
Trifenylfosfát byl nalezen v přírodě.[8] Triarylfosfáty se do vody mohou dostat odpařováním a úniky z plastů, případně z hydraulických kapalin nebo, v menší míře, z výroby;[4] konkrétně TPhP nalezený v životním prostředí pochází z průmyslu, výroby a použití v budovách, například v barvách a elektronických zařízeních.[11] Podobně jako jiné zpomalovače hoření založené na fosforu se TPhP může dostat do půdy, usazenin, prachu v budovách i do vzduchu.[4][10][13][14][15]
Ve vodě se TPhP rozkládá poměrně rychle, a to za aerobních i anaerobních podmínek.[4] I když se rozkládá rychle a nedochází u něj k bioakumulaci, tak jej lze snadno detekovat.[8]
Reference
V tomto článku byl použit překlad textu z článku Triphenyl phosphate na anglické Wikipedii.
- ↑ a b c d e f g h i j k l https://pubchem.ncbi.nlm.nih.gov/compound/8289
- ↑ a b Jürgen Svara; Norbert Weferling; Thomas Hofmann. Phosphorus Compounds, Organic. [s.l.]: Wiley-VCH, 2000-01-01. ISBN 9783527306732. DOI 10.1002/14356007.a19_545.pub2.
- ↑ Heather M. Stapleton; Susan Klosterhaus; Sarah Eagle; Jennifer Fuh; John D. Meeker; Arlene Blum; Thomas F. Webster. Detection of Organophosphate Flame Retardants in Furniture Foam and U.S. House Dust. Environmental Science & Technology. 2009-08-13, s. 7490–7495. DOI 10.1021/es9014019. PMID 19848166. Bibcode 2009EnST...43.7490S.
- ↑ a b c d Ike van der Veen; Jacob de Boer. Phosphorus flame retardants: Properties, production, environmental occurrence, toxicity and analysis. Chemosphere. 2012-08-01, s. 1119–1153. DOI 10.1016/j.chemosphere.2012.03.067. PMID 22537891. Bibcode 2012Chmsp..88.1119V.
- ↑ a b Emma Mendelsohn, Audrey Hagopian, Kate Hoffman, Craig M. Butt, Amelia Lorenzo, Johanna Congleton, Thomas F. Webster, Heather M. Stapleton. Nail polish as a source of exposure to triphenyl phosphate. Environment International. 2016-01-01, s. 45–51. DOI 10.1016/j.envint.2015.10.005. PMID 26485058.
- ↑ Triphenyl phosphate, found in 'eco-friendly' nail polish, spurs worries [online]. [cit. 2016-04-09]. Dostupné online.
- ↑ Quan Zhang; Chenyang Ji; Xiaohui Yin; Lu Yan; Meiya Lu; Meirong Zhao. Thyroid hormone-disrupting activity and ecological risk assessment of phosphorus-containing flame retardants by in vitro, in vivo and in silico approaches. Environmental Pollution. 2016-03-01, s. 27–33. DOI 10.1016/j.envpol.2015.11.051. PMID 26701863.
- ↑ a b c Zhongkun Du; Yan Zhang; Guowei Wang; Jianbiao Peng; Zunyao Wang; Shixiang Gao. TPhP exposure disturbs carbohydrate metabolism, lipid metabolism, and the DNA damage repair system in zebrafish liver. Scientific Reports. 2016-02-22, s. 21827. DOI 10.1038/srep21827. PMID 26898711. Bibcode 2016NatSR...621827D.
- ↑ Boris V. Krivoshiev; Freddy Dardenne; Adrian Covaci; Ronny Blust; Steven J. Husson. Assessing in-vitro estrogenic effects of currently-used flame retardants. Toxicology in Vitro. 2016-06-01, s. 153–162. DOI 10.1016/j.tiv.2016.03.006. PMID 26979758.
- ↑ a b c Quan Zhang; Meiya Lu; Xiaowu Dong; Cui Wang; Chunlong Zhang; Weiping Liu; Meirong Zhao. Potential Estrogenic Effects of Phosphorus-Containing Flame Retardants. Environmental Science & Technology. 2014-06-02, s. 6995–7001. DOI 10.1021/es5007862. PMID 24844797. Bibcode 2014EnST...48.6995Z.
- ↑ a b Triphenyl phosphate - Substance Information - ECHA [online]. [cit. 2016-04-09]. Dostupné v archivu pořízeném dne 2016-04-20.
- ↑ Rui Hou; Yiping Xu; Zijian Wang. Review of OPFRs in animals and humans: Absorption, bioaccumulation, metabolism, and internal exposure research. Chemosphere. 2016-06-01, s. 78–90. DOI 10.1016/j.chemosphere.2016.03.003. PMID 27010170. Bibcode 2016Chmsp.153...78H.
- ↑ Ruiwen He; Yunzi Li; Ping Xiang; Chao Li; Chunyang Zhou; Shujun Zhang; Xinyi Cui. Organophosphorus flame retardants and phthalate esters in indoor dust from different microenvironments: Bioaccessibility and risk assessment. Chemosphere. 2016-05-01, s. 528–535. DOI 10.1016/j.chemosphere.2015.10.087. PMID 26585356. Bibcode 2016Chmsp.150..528H.
- ↑ Mohamed Abou-Elwafa Abdallah; Adrian Covaci. Organophosphate Flame Retardants in Indoor Dust from Egypt: Implications for Human Exposure. Environmental Science & Technology. 2014-04-23, s. 4782–4789. DOI 10.1021/es501078s. PMID 24738854. Bibcode 2014EnST...48.4782A.
- ↑ Amina Salamova; Mark H. Hermanson; Ronald A .Hites. Organophosphate and Halogenated Flame Retardants in Atmospheric Particles from a European Arctic Site. Environmental Science & Technology. 2014-05-21, s. 6133–6140. DOI 10.1021/es500911d. PMID 24848787. Bibcode 2014EnST...48.6133S.
Externí odkazy
 Obrázky, zvuky či videa k tématu Trifenylfosfát na Wikimedia Commons
Obrázky, zvuky či videa k tématu Trifenylfosfát na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances
structure of triphenylphosphate
Space-filling model of the triphenyl phosphate molecule



