Trimethylfosfin
| Trimethylfosfin | |
|---|---|
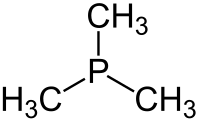 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | trimethylfosfan |
| Funkční vzorec | (CH3)3P |
| Sumární vzorec | C3H9P |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 594-09-2 |
| EC-no (EINECS/ELINCS/NLP) | 209-823-1 |
| PubChem | 68983 |
| ChEBI | 35890 |
| SMILES | CP(C)C |
| InChI | InChI=1S/C3H9P/c1-4(2)3/h1-3H3 |
| Vlastnosti | |
| Molární hmotnost | 76,077 g/mol |
| Teplota tání | −85 °C (188 K)[1] |
| Teplota varu | 37,5 °C (310,6 K)[1] |
| Hustota | 0,735 g/cm3 |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v dibutyletheru |
| Bezpečnost | |
| [1] | |
| H-věty | H225 H315 H319 H335[1] |
| P-věty | P210 P233 P240 P241 P242 P243 P261 P264 P271 P280 P302+352 P303+361+353 P304+340 P305+351+338 P312 P321 P332+313 P337+313 P362 P370+378 P403+233 P403+235 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
Trimethylfosfin je organická sloučenina fosforu se vzorcem P(CH3)3, zkráceně psaným jako PMe3. Jedná se o bezbarvou kapalinu se silným zápachem, podobným jako u ostatních alkylfosfinů. Používá se jako ligand v koordinační chemii.
Struktura
Tato sloučenina má pyramidální molekuly s grupou symetrie C3v. Úhly vazeb C–P–C jsou okolo 98,6°;[2] odpovídají tak tomu, že fosfor využívá k tvorbě vazeb převážně orbitaly 3p a téměř nedochází k sp hybridizaci atomu fosforu. Volný elektronový pár tak má převážně vlastnosti orbitalu s, podobně jako u fosfanu, PH3.[3]
PMe3 lze připravit reakcí trifenylfosfitu s methylmagnesiumchloridem:[4]
- 3 CH3MgCl + P(OC6H5)3 → P(CH3)3 + 3 C6H5OMgCl
Reakce se provádí v dibutyletheru, z něhož se těkavější PMe3 oddestiluje.
Reakce

Při pKa o hodnotě 8,65 reaguje PMe3 se silnými kyselinami vratně za vzniku solí [HPMe3]X.[2] Za přítomnosti silných zásad, jako jsou alkyllithných sloučenin se methylová skupina deprotonuje za tvorby PMe2CH2Li.
PMe3 lze snadno oxidovat kyslíkem na fosfinoxid. Reaguje s methylbromidem za tvorby tetramethylfosfoniumbromidu.[6]
Koordinační chemie
Trimethylfofosfin je silně zásaditý ligand, který může tvořit komplexy. Jako ligand má Tolmanův úhel 118°.[7] Tento úhel naznačuje míru sterické ochrany, kterou ligand poskytuje kovu, na nějž je navázán.
Na jeden atom kovu se může navázat více trimethylfosfinových ligandů, jako je tomu v komplexu Pt(PEt3)4.[8]
Komplex s jodidem stříbrným, AgI(PMe3), je na vzduchu stálá pevná látka, která zahřátím uvolňuje PMe3.[9]
Bezpečnost
PMe3 je toxický a samozápalný. Lze jej přeměnit na bezpečnější fosfinoxid reakcí s chlornanem sodným nebo peroxidem vodíku.[10]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Trimethylphosphine na anglické Wikipedii.
- ↑ a b c d e https://pubchem.ncbi.nlm.nih.gov/compound/68983
- ↑ a b Annette Schier and Hubert Schmidbaur"P-Donor Ligands" in Encyclopedia of Inorganic Chemistry 2006, Wiley-VCH, Weinheim. doi:10.1002/0470862106.ia177
- ↑ E. Fluck, The chemistry of phosphine, Topics in Current Chemistry Vol. 35, 64 pp, 1973.
- ↑ M. L. Leutkens; A. P. Sattelberger; H. H. Murray; J. D. Basil; J. P. Fackler. Trimethylphosphine. Inorganic Syntheses. 1990, s. 305–310. ISBN 9780470132593. doi:10.1002/9780470132593.ch76.
- ↑ A. Sattler; G. Parkin. Formation of a cationic alkylidene complex via formal hydride abstraction: synthesis and structural characterization of [W(PMe3)4(η2-CHPMe2)H]X (X = Br, I). Chemical Communications. 2011, s. 12828–12830. doi:10.1039/C1CC15457E. PMID 22048609.
- ↑ H. F. Klein. Inorganic Syntheses. [s.l.]: [s.n.], 1978. ISBN 9780470132494. doi:10.1002/9780470132494.ch23. Kapitola Trimethylphosphonium Methylide (Trimethyl Methylenephosphorane), s. 138–140.
- ↑ G. L. Miessler and D. A. Tarr Inorganic Chemistry, 3rd Ed, Pearson/Prentice Hall publisher, ISBN 0-13-035471-6
- ↑ T. Yoshida, autor2 = T. Matsuda; S. Otsuka. Inorganic Syntheses. [s.l.]: John Wiley & Sons, 1990. ISBN 9780470132593. doi:10.1002/9780470132593.ch32. Kapitola Tetrakis(Triethylphosphine)Platinum(0), s. 122–123.
- ↑ EDWARDS, H.G.M.; FARWELL, D.W. The vibrational spectrum of trimethylphosphine-silver iodide, [AgI·P(CH3)3]4. Journal of Molecular Structure. 1989-06-01, roč. 197, s. 203–212. Dostupné online [cit. 2025-04-10]. doi:10.1016/0022-2860(89)85163-4. (anglicky)
- ↑ http://www.sigmaaldrich.com/catalog/product/aldrich/324116?lang=en®ion=US&cm_sp=Insite-_-prodRecCold_xorders-_-prodRecCold2-2
Externí odkazy
 Obrázky, zvuky či videa k tématu Trimethylfosfin na Wikimedia Commons
Obrázky, zvuky či videa k tématu Trimethylfosfin na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for flammable substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Ball-and-stick model of the trimethylphosphine molecule, P(CH3)3
Structure calculated using HF/6-31G* in Spartan '04 Student Edition. Image generated in Accelrys DS Visualizer.Strukturformel von Trimethylphosphin






