Vazba sigma

Vazba sigma (σ) je druh kovalentní chemické vazby, který vzniká, když dojde k maximálnímu překryvu atomových orbitalů na spojnici středů jader vázaných atomů; jedná se o nejsilnější druh kovalentní vazby.[1]
Nejsnadněji se tento typ vazby definuje pro dvouatomové molekuly, a to pomocí grup symetrie. Vazba sigma je symetrická s ohledem na rotaci vazebné osy. Podle této definice jsou běžnými podtypy s+s, pz+pz, s+pz a dz2+dz2 (kde z je osa vazby, tedy osa kolmá na spojnici středů jader).[2]
Podle kvantové teorie dochází k hybridizaci molekulových orbitalů se shodnými symetriemi. Důsledkem tohoto jevu je splynutí vlnových funkcí orbitalů s+s a pz+pz.

U molekul složených ze dvou atomů stejného prvku se nevyskytují uzlové roviny, ve kterých by vlnová funkce měla nulovou hodnotu, a to ani mezi vázanými atomy, ani uvnitř nich. Odpovídající protivazebný orbital σ* je definován přítomností jedné uzlové roviny mezi oběma vázanými atomy.
Vazby sigma jsou ze všech kovalentních vazeb nejsilnější, protože zde dochází k přímému překryvu orbitalů. Elektrony podílející se na vazbě sigma se často označují jako sigma elektrony.[3]
Při pohledu směrem dolů na osu vazby má molekulový orbital σ kruhovou symetrii, která odpovídá atomovému orbitalu „s“.
Jednoduchá vazba je obvykle typu sigma, zatímco násobné vazby se skládají z vazby sigma a jedné či více vazeb jiných typů (například pí). Dvojná vazba je složena z jedné vazby sigma a jedné vazby pí, trojná z jedné vazby typu sigma a dvou typu pí.
| —— | ———————————————— | ————— |
Atomové orbitaly |  | |
| Souměrné (s–s a p–p) vazby sigma mezi atomovými orbitaly | Vazba pí (pro porovnání) | |
| —— | ———————————————— | ————— |
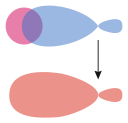 σhybridizovaný orbital s | 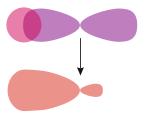 σs–p | |
Vazba σ u molekul s více než 2 atomy
Myšlenku vzniku vazeb σ přímým překryvem atomovým orbitalů s lze rozšířit na interakce vytvořené překryvem jednoho laloku prvního a jednoho laloku druhého atomového orbitalu jiných typů; například v molekule propanu se vyskytuje 10 vazeb σ – dvě vazby C-C a 8 vazeb C-H.
Vazba σ u vícevazných komplexů
Komplexy přechodných kovů obsahující vícenásobné vazby, například dihydrogenkomplexy mají vazby sigma mezi atomy vázanými vícenásobnými vazbami. Tyto vazby se mohou kombinovat s ostatními typy vazeb jako jsou vazby π, jako například v molekule W(CO)3(PCy3)2(H2) a dokonce, jako například u octanu chromnatého,[4] i s vazbami δ.
Vazba σ v organických molekulách
V molekulách mnoha organických sloučenin, jako je benzen, se vyskytuje jeden či více cyklů; tyto cykly se mnohdy skládají z vazeb typu sigma a pí. Počet vazeb sigma je roven součtu počtu atomů a počtu cyklů zmenšenému o 1.
Necyklickou molekulu lze zobrazit jako strom s počtem vazeb rovným počtu atomů zmenšenému o jednotku (například v dvouatomové molekule vodíku, H2, je jen jedna vazba sigma a v molekule amoniaku, NH3, jsou takové vazby tři). Mezi dvěma atomy nemůže být více než jedna vazba σ.
Cyklické molekuly mají další vazby σ, například benzen má mezi 6 uhlíkovými atomy v cyklu 6 vazeb tohoto typu. V molekule antracenu C14H10 jsou tři cykly, a podle výše uvedeného pravidla se tam tedy nachází 24 + 3 − 1 = 26 vazeb sigma; zde jde o 16 vazeb C-C a 10 vazeb C-H.
Odkazy
Související články
Reference
V tomto článku byl použit překlad textu z článku Sigma bond na anglické Wikipedii.
- ↑ John Moore; Conrad L. Stanitski; Peter C. Jurs. Principles of Chemistry: The Molecular Science. [s.l.]: [s.n.], 21. 1. 2009. Dostupné online. ISBN 9780495390794. (anglicky)
- ↑ Jonathan Clayden; Nick Greeves; Stuart Warren. Organic Chemistry. Oxford: OUP Oxford, 3. 2012. (2). Dostupné online. ISBN 978-0199270293. S. 101–136. (anglicky)
- ↑ James Keeler; Peter Wothers. Chemical Structure and Reactivity. Oxford: OUP Oxford, 5. 2008. (1). Dostupné online. ISBN 978-0199289301. S. 27–46. (anglicky)
- ↑ Gregory Kubas. Metal Dihydrogen and σ-Bond Complexes: Structure, Theory, and Reactivity. Journal of the American Chemical Society. 2002, s. 3799–3800. (anglicky)
Média použitá na této stránce
Autor:
- derivative work: הגמל התימני (talk)
- Electron_orbitals.svg: Patricia.fidi
Electron orbitals
Molecular orbital of hydrogen fluoride
The 1s σ* antibonding molecular orbital of the dihydrogen molecule, H2
s-q molecular orbital
Autor: SVG: ZooFari; Raster: Anselm H. C. Horn, Licence: CC BY-SA 3.0
σ bond between two atoms : localisation of electronic density.




