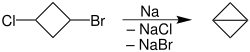Wurtzova reakce
Wurtzova reakce je reakce v organické a organokovové chemii a u anorganických polymerů, při níž reagují dva halogenalkany se sodíkem v etherovém roztoku za tvorby vyššího alkanu. Slouží především k tvorbě alkanů se sudými počty atomů uhlíku:
- 2 R−X + 2 Na → R−R + 2 Na+X−
Ke zlepšení účinnosti reakce lze použít i jiné kovy, jako jsou stříbro, zinek, železo, aktivovaná měď a indium.[1] Wurtzovy reakce probíhají radikálově, což vyvolává vedlejší reakce vytvářející alkeny.
Podobnou reakcí, využívající arylhalogenidy, je Wurtzova–Fittigova reakce.
Mechanismus
Reakce začíná výměnou kovu a halogenu probíhající přes radikál R· (podobně jako při tvorbě Grignardových činidel) za tvorby vazby uhlík–uhlík nukleofilní substitucí.
Jeden elektron se přesune z kovu na halogen za vzniku halogenidu a alkylového radikálu:
- R−X + M → R· + M+X−
Tento radikál následně přijme elektron z jiného atomu kovu a vytvoří alkylový anion:
- R· + M → R−M+
Výsledný meziprodukt lze v některých případech izolovat.
Nukleofilní alkylový anion následně odštěpí halogenid v SN2 reakci za tvorby nové kovalentní vazby uhlík–uhlík:
- R−M+ + R−X → R−R + M+X−
Podmínky a příklady
Vzhledem ke svým omezením, jako je úzké rozmezí použitelných funkčních skupin. Wurtzova reakce je ovšem vhodná k tvorbě malých, obzvláště tříčlenných, kruhů. Takto byl například připraven bicyklobutan z 1-brom-3-chlorcyklobutanu, s 95% výtěžností. Reakce byla provedena v dioxanu za teploty refluxu, kdy je sodík kapalný. Reakce měla nízkou výtěžnost, protože se vytvářelo několik produktů.
U 1,3-, 1,4-, 1,5- a 1,6-dihalogenidů se vytváří cyklické sloučeniny. Při použití vicinálních dihalogenidů vznikají alkeny a u geminálních alkyny.[2]
Omezení
Wurtzova reakce má kvůli četným vedlejším reakcím jen omezené využití.[3] Ojediněle se používá na přípravu symetrických alkanů. Pokud se použijí dva různé alkylhalogenidy, tak se vytvoří směs alkanů často obtížně rozdělitelná frakční destilací, protože rozdíly v teplotách varu produktů bývají malé. Tímto způsobem nelze získat methan. Reakce také neprobíhá u terciárních halogenidů. Vzhledem k tomu, že se při níž tvoří radikály, tak také dochází k vedlejším reakcím vytvářejícím alkeny. Vliv vedlejších reakcí je větší tehdy, když alkylhalogenidové skupiny vytváří významné sterické efekty.
Odkazy
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu Wurtzova reakce na Wikimedia Commons
Obrázky, zvuky či videa k tématu Wurtzova reakce na Wikimedia Commons
Literatura
- Adolphe Wurtz. Sur une nouvelle classe de radicaux organiques. Annales de chimie et de physique. 1855, s. 275–312. Dostupné online. (anglicky)
- Adolphe Wurtz. Ueber eine neue Klasse organischer Radicale. Annalen der Chemie und Pharmacie. 1855, s. 364–375. Dostupné online. DOI 10.1002/jlac.18550960310. (anglicky)
- Organic-chemistry.org
Reference
V tomto článku byl použit překlad textu z článku Wurtz reaction na anglické Wikipedii.
- ↑ March Advanced Organic Chemistry 4th edition p. 535.
- ↑ Gary M. Lampman and James C. Aumiller "Bicyclo[1.1.0]butane" Organic Syntheses, 1971, volume 51, pp 55-9. DOI:10.15227/orgsyn.051.0055 Aditya Krishna "Dihalides Quartz"
- ↑ March Advanced Organic Chemistry 7th edition p. 512
Média použitá na této stránce
Structure of the synthesis of bicyclobutanes