Ethylene-CRC-MW-dimensions-2D
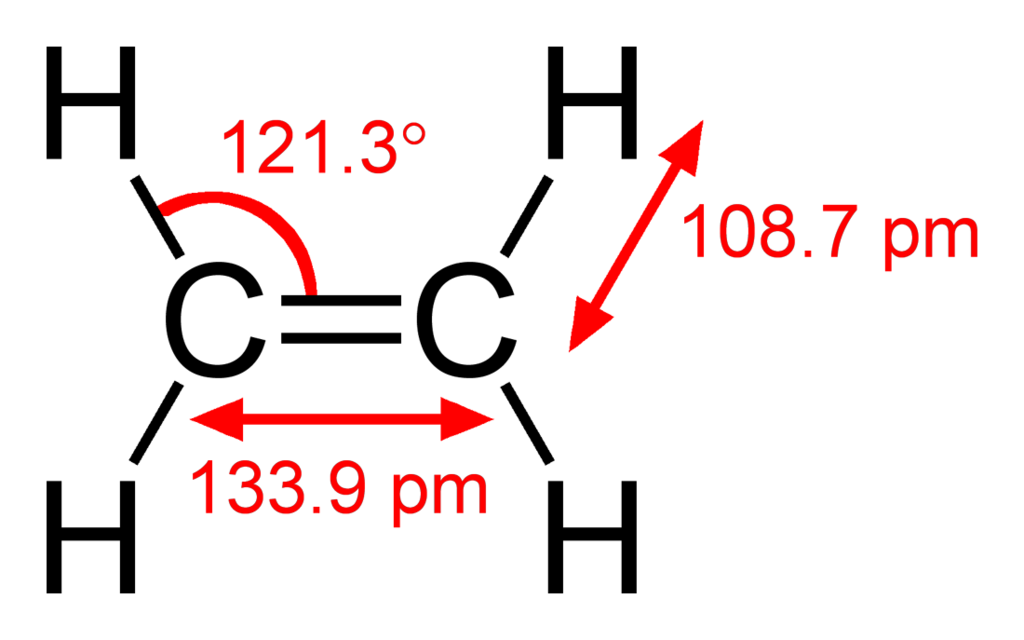
Structural formula of the ethylene (ethene) molecule, C2H4. The molecule belongs to the D2hpoint group.
Structural information (determined by microwave spectroscopy) from CRC Handbook, 88th edition.| Benjah-bmm27, autor tohoto díla, jej uvolnil jako volné dílo, a to celosvětově. V některých zemích to není podle zákona možné; v takovém případě: |
Relevantní obrázky
Relevantní články
Dvojná vazba (chemie)Jako dvojná vazba se v chemii označuje chemická vazba mezi dvěma atomy, jíž se účastní čtyři vazebné elektrony namísto obvyklých dvou. Nejčastější dvojnou vazbu, mezi dvěma atomy uhlíku, lze nalézt v alkenech. Existuje mnoho typů dvojných vazeb mezi různými prvky; například v karbonylové skupině mezi atomem uhlíku a atomem kyslíku. Jinými hojně rozšířenými dvojnými vazbami jsou vazby v azosloučeninách (N=N), iminech (C=N) a sulfoxidech (S=O). Ve strukturních vzorcích se dvojná vazba znázorňuje dvěma rovnoběžnými čarami mezi atomy. Mezi stejnými dvěma atomy je dvojná vazba obecně silnější a kratší než vazba jednoduchá. Pokud molekula obsahuje dvě nebo více dvojných vazeb, označujeme je podle polohy jako kumulované, konjugované nebo izolované. .. pokračovat ve čtení
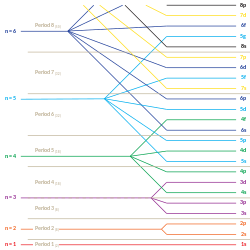
Hybridizace orbitalůHybridizace orbitalů je proces energetického sjednocení původně energeticky nerovnocenných atomových orbitalů. Celková energetická hladina orbitalů se však po hybridizaci nezmění a je tedy zachováno energetické těžiště orbitalů. Tyto orbitaly se nazývají hybridní orbitaly. .. pokračovat ve čtení
Vazba píVazba pí (π) je kovalentní vazba, při níž se dva laloky jednoho atomového orbitalu překryjí se dvěma laloky orbitalu jiného atomu a spojnice středů jader vázaných atomů neprochází těmito překryvy. Na společné uzlové rovině, která prochází jádry vázaných atomů, je nulová elektronová hustota a tato rovina je i uzlovou rovinou molekulového orbitalu vzniklé vazby. .. pokračovat ve čtení
Vazba uhlík–vodíkVazba uhlík-vodík (C–H) je kovalentní vazba mezi atomy uhlíku a vodíku; vyskytuje se v mnoha organických sloučeninách. Jeden uhlík může sdílet své valenční elektrony až se čtyřmi atomy vodíku, čímž atomy dosáhnou elektronové konfigurace vzácného plynu. Obvyklé délky těchto vazeb jsou okolo 109 pm a vazebné energie kolem 413 kJ/mol. Vzhledem k tomu, že elektronegativita má u C hodnotu 2,55 a u H 2,2, tak se vazby C−H v důsledku malých rozdílů elektronegativity mezi vázanými atomy obvykle považují za nepolární. Ve strukturních vzorcích organických sloučenin se atomy vodíku často nezobrazují. Ke sloučeninám obsahujícím pouze vazby C–H a C–C patří alkany, alkeny, alkyny a areny, sloučeniny souhrnně označované jako uhlovodíky. .. pokračovat ve čtení
Vazba uhlík–uhlíkVazba uhlík–uhlík je kovalentní vazba mezi dvěma atomy uhlíku. .. pokračovat ve čtení